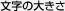消化器外科
どんな病気を扱っているの?(肝臓、膵臓、胆嚢)
はじめに 当院の肝切除術の実施状況
当科では、原発性肝癌、胆管癌、転移性肝癌などの肝腫瘍に対し肝切除術を実施しております。肝切除術は術中・術後出血、術後肝不全などを併発する可能性のある手術です。当院での手術は肝胆膵高度技能指導医、肝胆膵高度技能専門医の執刀の元、安全に切除できる様に体制を整えています。さらに、術前、術後の患者様の管理につきましても肝臓専門医の消化器内科と緊密に連携し安全に手術を受け、退院していただけるよう努力しております。
また、近年導入されております腹腔鏡下肝切除術も積極的に実施しており、内視鏡外科学会技術認定医の執刀の元、安全に施行しております。
肝切除についての質問、手術適応、術式選択についての質問は、消化器外科の肝胆膵専門医にお聞きください。
肝がんについて
肝細胞癌とは
肝臓に発生する癌には、肝臓自体から発生する原発性肝癌と、肝臓以外の臓器から発生した癌が肝臓に転移する転移性肝癌があります。原発性肝癌の代表的なものに、肝細胞から発生する肝細胞癌と肝臓内の胆管細胞から発生する肝内胆管癌(胆管細胞癌)があり、頻度は肝細胞癌が全体のおよそ95%を占め、肝内胆管癌は4.5%と稀で、一般的に肝癌といえばこの肝細胞癌を示します。
肝切除術の対象となる疾患には下記のようなものがあります。
- 原発性肝癌(肝細胞癌、胆管細胞癌、混合型肝癌など)
- 胆道癌(肝門部胆管癌、胆嚢癌、上・中・下部胆管癌など)
- 転移性肝癌(大腸癌からの肝転移など)
- 良性腫瘍(肝血管腫、肝線種、肝嚢胞 など)
- 肝膿瘍 など
肝細胞癌の発生原因
わが国の肝細胞癌の原因は、約90%が肝炎ウイルス、すなわちB型やC型肝炎ウイルスの感染が関与し、その内訳はC型肝炎ウイルス(HCV)が約70%、B型肝炎ウイルス(HBV)が約20%です。肝炎ウイルスが肝臓に持続的に感染することで肝炎(慢性肝炎)が起こり、肝臓の正常な細胞が死滅・再生を繰り返し線維化が進行します。この線維化が高度となると肝硬変となります。このような線維化の過程でがん遺伝子やがん抑制遺伝子の影響を受けて、肝細胞癌が起こるといわれています。その他の肝細胞癌の原因としてアルコールがあります。多量のかつ持続的なアルコール摂取により肝細胞が障害を受け、その修復過程において遺伝子に傷が入ることが発癌のきっかけとなります。また最近ではアルコール摂取がないにもかかわらず脂肪肝から脂肪肝炎を生じ(非アルコール性脂肪肝炎NASH(ナッシュ):Non-alcoholic steatohepatitis)その過程で肝細胞癌が生じることがわかっていて近年増加傾向です。NASHはいわゆるメタボリック症候群と呼ばれる肥満、糖尿病、高血圧、高脂血症を合併することが多く何らかの関係がありそうですが、NASHや発癌のメカニズムについてはまだ解明されていません。
肝細胞癌の診断・進行度
肝臓は“沈黙の臓器”といわれ、肝細胞癌に特異的な症状はありません。肝細胞癌が増大し腹部に触れるようになる、破裂して腹痛が起こるといった稀な事例はありますが、基本的には症状はありません。そのため肝細胞癌を見つけるためには自ら進んで検査を受けることが大切です。肝炎ウイルス感染( B および C 型肝炎ウイルス)、大量飲酒、喫煙、メタボリックシンドローム(糖尿病、高血圧)のような因子を持っている人は定期的に肝臓を診てもらうことが必要です。この中でHCVおよびHBVに感染している人(慢性肝炎)は肝細胞癌が発症しやすいハイリスクグループに属しているため定期検診が必要となります。また、常習的に飲酒をしている人、NASHの人も定期検診を受けることをお勧めします。
◎C型肝炎のハイリスク群
C型肝炎では、慢性肝炎から肝硬変へと進行する際に起こる線維化は緩徐かつ段階的に進行し、線維化の進行とともに発癌率が上昇することがわかっています。線維化の程度(線維化ステージ)は新犬山分類(F0~F4まで分類)が用いられ、F0は線維化なし、F1~3が慢性肝炎、F4が肝硬変、となります。F0~F4の診断は、超音波下で細い針を用いて肝臓の一部の組織を採取し(肝生検)、病理学的検査(顕微鏡で診断すること)で行われます。また簡便な診断方法として、血液検査での血小板数が肝臓の線維化と相関することがわかっており、血小板が18万前後でF1、13万以下でF3、10万以下になるとF4と推定されます。今後10年間での発癌する確率は、F1:約5 %未満、F2:約20 %、F3:約50 %、F4:約70 %と報告されています。
◎B型肝炎のハイリスク群
B型慢性肝炎も肝硬変になると10年間で約50%の発癌率があります。C型に比べて、若い年令で線維化が進行していなくても発癌する場合があるので注意が必要です。
肝細胞癌を発見するための検査手順は二段階になっています。第一段階は肝細胞癌になりやすい人を見つける検査で、第二段階は肝細胞癌の診断と進行度を確定する検査です。第一段階の検査には、肝機能やウイルス性肝炎に関わる血液検査、腹部超音波検査があります。これらの検査結果から精密検査が必要と判断された場合には、血液検査での腫瘍マーカー(AFP、AFP-L3分画、PIVKA-II)のチェック、腹部造影超音波検査、CTスキャン、MRI(特にGd-EOB-MRI)、血管造影検査などの画像検査を行います。肝細胞癌の特徴的なことは、初期の段階では正常肝臓と同じように肝動脈と門脈による二重の血流支配を受けていますが、その進行とともに動脈のみから支配を受けるようになり、血管増生に富む腫瘍となることです。肝細胞癌の診断にはこれらの血流支配の特殊性が考慮されます。
肝細胞癌の進行度は、原発性肝癌取扱い規約により、T因子(腫瘍の病態)、N因子(リンパ節転移の有無)、M因子(遠隔転移の有無:肺、骨転移など)の三つの因子によって決定されます(図1)。T因子は、【1】腫瘍が1個だけ(単発)、【2】大きさが2cm以下、【3】門脈・肝静脈・胆管への癌の浸潤がなし、の3項目により、T1:3項目合致、T2:2項目合致、T3:1項目合致、T4:すべて合致せず、と取り決められています。
ステージ I はT1N0M0、ステージ II はT2N0M0、ステージIIIはT3N0M0、ステージIVは IVA と IVB の二つに分けられ、遠隔転移があれば IVB となり、IVA はT4N0M0、または T1、2、3、4のいずれか、かつ N1M0 となります(図2)。

肝細胞癌の治療
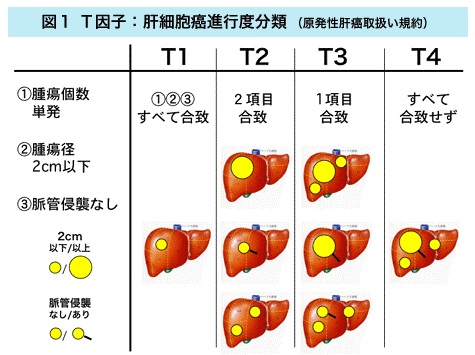
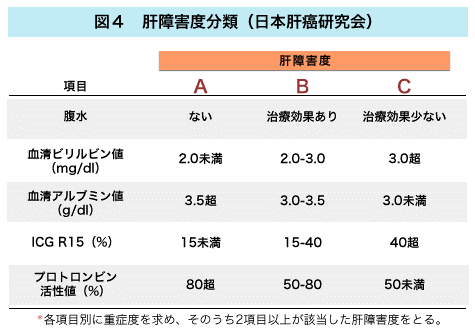
肝細胞癌の治療は、1)手術療法、2)局所療法(エタノール注入療法、マイクロ波凝固療法、ラジオ波焼灼療法)、3)血管塞栓療法、4)肝動注療法、および5)肝移植があります。最近では、分子標的治療薬が肝細胞癌の治療として認められ、進行した症例に対し導入されます。肝細胞癌の治療方針の決定には、全身状態も考慮された上で、基本的に“肝癌診療ガイドライン“のアルゴリズムを参考にします(図3)。このアルゴリズムは、宿主因子(肝機能)と腫瘍因子(腫瘍個数と腫瘍の大きさ)により構成され、例えば肝機能が比較的良好、すなわち肝障害度(図4:肝臓の機能の評価に用いる)がAまたはBで3個以内の肝細胞癌に対しては肝切除または局所療法が推奨されます。また肝細胞癌が4個以上であれば肝動脈塞栓療法が推奨され、肝機能が不良(肝障害度C)の場合は肝移植や緩和医療が適応となります。
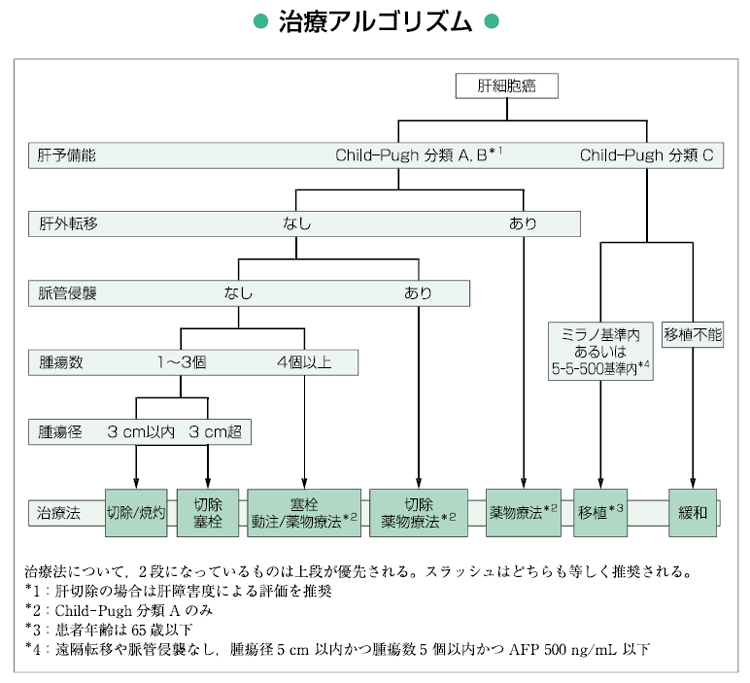
肝癌診療ガイドライン 2021年版
胆管細胞癌について
胆管細胞癌(肝内胆管癌)とは
肝内に発生した胆管上皮に似る、あるいはそれに由来する細胞からなる上皮性悪性腫瘍です。原発性肝癌の約5%を占めます。病因としては、肝内結石症、原発性硬化性胆管炎、肝吸虫症、トロトラストなどとの因果関係を指摘されていますが、詳細は明らかにされていません。肝細胞癌のように、ハイリスクグループの同定が困難であり、早期発見が難しい疾患で、腫瘍がある程度大きくなって発見されることが多いのが特徴です。ただし、HBVが7.3%、HCVが24.7%で陽性と、一般に比べれば肝炎ウィルスマーカーの陽性率が高いことが知られています。臨床症状は、肝細胞癌と同様、特徴的な症状はありません。腫瘍マーカーとしては、CEA、CA 19-9が代表的なものです。肝細胞癌と同様に超音波、CTスキャン、MRI、血管造影などの画像診断がなされます。肝細胞癌と異なる点は、血管増生に乏しいという点です。また胆管への進展度を評価するために、MRIを利用したMRCPという、造影剤を使用せずに胆管像を描出できる検査も行います。これで評価できない場合は、直接胆管に造影剤を注入する方法(ERCP:内視鏡を用いた胆管造影、PTC造影:超音波下に、皮膚の上から胆管に細い管を留置し行う)を行うこともあります。
胆管細胞癌(肝内胆管癌)の治療
胆管細胞癌は腺癌で、胃癌や大腸癌と似た発育をします。このため、治療法としては、切除が基本となります。肝障害がないことが多いため、肝細胞癌より肝切除量の制限が少ないですが、腫瘍が大きいことが多く、進展様式が多彩なため、それらを考慮した切除が必要になります。例えば、肝細胞癌と異なりリンパ節に転移しやすいなどの特徴があり、所属するリンパ節を「郭清」といって、一緒に取り除く手術を行います。切除できない場合は、抗癌剤治療などが行われます。
転移性肝癌について
転移性肝癌とは
転移性肝癌は、肝腫瘍の中で最も頻度が高い腫瘍です。肝臓は肺に次ぐ転移の好発臓器であり、悪性腫瘍は発生部位や種類に関わらず肝転移を来たす可能性をもちます。
特に経門脈性転移が起こりやすい腹部消化器癌において肝臓は、転移先として最初に標的となる臓器と考えられます。
1.外科的治療法(肝切除術)
□ 外科的治療の条件
外科的治療法は、癌を切除することで肝臓から腫瘍を除去することが可能なる最も確実な方法です。転移性肝癌に対する肝切除の適応は次のような条件を満たした場合に検討されます。
- 安全な肝切除量の範囲内で転移巣が完全に切除できること。
- 原発巣を含めた他臓器病変が外科的に制御可能であること。
また腫瘍の大きさや数が多く広範囲の切除が必要となる場合、この切除許容範囲は患者さん自身の肝予備能(体を維持するための本来の肝機能の能力)により決定され、肝予備能が不良の場合、切除範囲は制限されます。現在当科では、ICG-R15およびアシアロシンチグラムという検査の値を参考にして肝臓の切除量を決定しています。原発臓器による特徴については後述します。
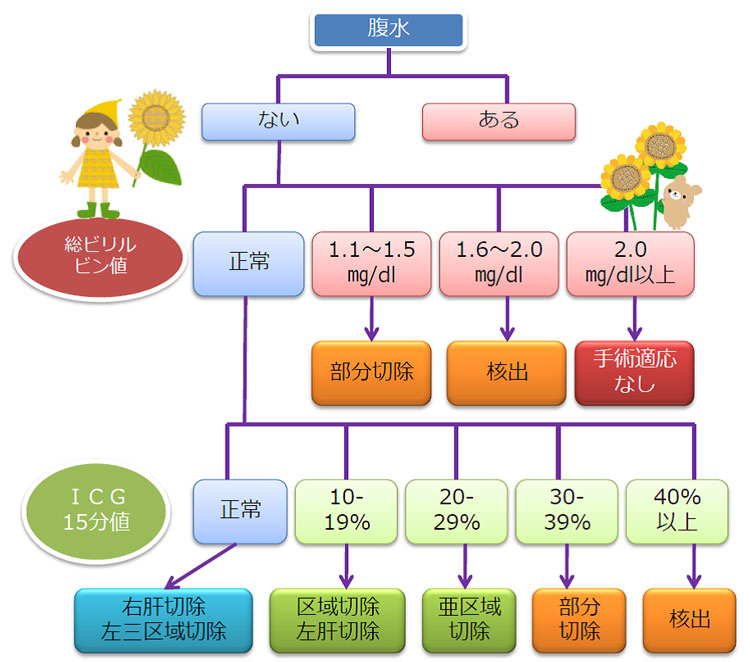
【 術 式 】
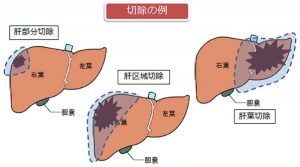
術式は、肝臓の切除範囲によって以下のように分けられます。
部分切除・亜区域切除・区域切除・葉切除・拡大葉切除。
また手術操作の必要に応じ胆嚢を同時に摘出することもあります。
 |
 |
【腹腔鏡下肝切除術】
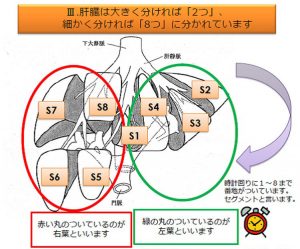
肝癌に対する肝切除術は、肝臓の解剖学的理由(右肋骨の奥に存在し、背中側に固定され、非常に血流の豊富な出血しやすい臓器である)から、従来、下記のような大開腹(40cm以上の皮膚切開)を余儀なくされ、肝切除が安全に行われるようになった今日でも患者さんにとっての大きなデメリットでした。腹腔鏡下肝切除術は1991年に世界で初めて施行され、本邦では1993年に初めて施行された後、徐々に症例数が増加してきました。昨今の手術器具の進歩に伴い、腹腔鏡下肝切除術は、さらに安全で低侵襲な手技となり、2000年に高度先進医療、2006年に先進医療となり、2010年4月には施設に対する条件付きで保険診療として認められました。
当科でも、腹腔鏡下肝切除を積極的に行い肝切除術の低侵襲化に取り組んでいます。
腹腔鏡下肝切除術は、開腹創を全く設けない完全腹腔鏡下肝切除術と、腹腔鏡を補助的に使用し開腹創を最小限(10~15cmの皮膚切開)にする腹腔鏡補助下肝切除術に大別されます。当科では、個々の症例での肝癌の部位や大きさを考慮し、手術の安全性、癌の根治度を担保することを第一に、可能な限り開腹創を小さくし、体への負担を小さくする低侵襲手術を行っています。(再肝切除または開腹歴のある患者様では、腹腔内の癒着の程度などを考慮し、手術方針を決定しています) これまでの臨床経験で、腹腔鏡下肝切除術においては術後鎮痛剤の使用回数の軽減、入院期間短縮などのメリットがあることが示されています。
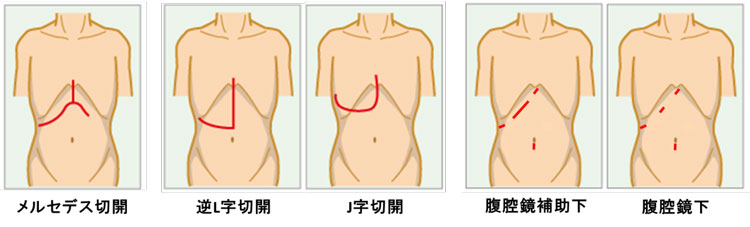
肝切除に適応される皮膚切開
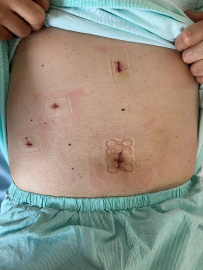
手術創写真 (完全腹腔鏡下)
完全腹腔鏡下肝切除術では、内視鏡および鉗子の挿入ポートのみの傷となり、術後の疼痛などが顕著に緩和され、早期退院も可能になっています
□ 一期的に肝切除を行うと肝切除量が大量となり肝不全が懸念されるような場合
転移性肝癌の数または広がりが広範囲なため、安全な肝切除量の範囲内での転移巣の完全切除が困難な場合があります。しかし現時点では転移巣の根治性を最も期待できる治療法は肝切除であると考えられます。
このため当科では、外科的に切除できる機会をできるだけ増やし、転移性肝癌に対する治療成績を向上させようと努力しています。具体的には次にあげる4つの方法を検討しています。
- 化学療法によるdownstaging + 肝切除術:
まず化学療法を行なって転移巣の容積を縮小させることによって、転移巣を完全に切除するのに必要な肝切除量を減少させる方法です。 - 門脈塞栓術(PTPE) (残肝の大きさ<35%のとき) + 肝切除術
肝臓には、門脈と肝動脈が流入しています。このうち左右いずれかの門脈を塞栓すると反対側の肝葉が約10%腫大することが期待されます。この方法で術前に残肝の容積を大きくして肝切除をする方法です。 - 肝切除術+ラジオ波焼灼療法(RF)
転移巣のうち、主病巣を切除しても残肝内の腫瘍が3個以内,大きさ3cm以下 の範囲内で残存する場合にラジオ波焼灼療法を併用して残肝の腫瘍も治療する方法です。 - 2期的肝切除術
肝臓は、大量に切除しても残肝が腫大して約3週間後にはほぼ元の大きさに戻ると云われています。転移巣のうち、主病巣を切除しても残肝内の腫瘍が3 個以上、大きさ3cm以上であった場合、まず主病巣を切除後残肝の腫大を待って2期的に残肝内の転移巣を切除する方法です。
□ 再々発転移性肝腫瘍に対する再肝切除について
転移性肝癌に対して肝切除後の再発例に対する再肝切除率は諸外国で5〜10%、本邦では18%であり、手術が選択肢の一つと考えられています。さらに5年生存率も、21〜48%と初回肝切除例と同等となってきています。
当科では肝切除後再発例に対する再肝切除も積極的に取り組んでいく方針です。
原発臓器別の特徴について
転移性肝癌の代表的な原発臓器別の治療について説明します。
大腸癌
大腸・直腸癌の肝転移術後の5年生存率は25%から40%と諸家から報告されていますが、Stage IVという進行度からすると良好な成績であるといえます。腹部の消化器の血液は一度肝臓を通ってから全身に回るため、肝転移は肝臓というフィルターで癌細胞がひっかかり発育した状態と考えることができ、他の臓器への転移の一歩手前の段階で見つかったと考えられるためです。従って大腸直腸癌からの肝転移に対しては肝切除が最も良い治療と考えています。ただし肝転移症例すべてが肝切除の適応となるわけではありません。肝外病変、例えば肝門部リンパ節に転移がある場合は肝切除術を行っても長期生存が望めません。このような症例を除いて、手術はあくまで安全にしかも確実に全ての腫瘍が切除可能と判断される場合に行われます。正常肝の場合、非腫瘍部分の肝容量が35%以上残り、かつ腫瘍を全て除去できる場合に切除可能と判断します。肝切除後に残った肝臓に再発した場合は再度肝切除を追加することが最良と考えられます。
胃癌
肝転移を伴う胃癌の4割は腹膜播種を併存し、また6割が肝両葉にわたり転移巣を認めるため、肝切除の適応となるのは全体の1割程度です。しかしこのような場合、肝切除の治療成績は大腸癌と同等との報告もあり、手術適応例には積極的に切除をする方針です。肝切除の適応は、1)同時性と異時性を問わず、肝転移個数が1個で、腹膜播種および大動脈周囲リンパ節転移がない。2)異時性肝転移の場合は胃癌そのものが組織学的にリンパ管あるいは脈管侵襲がないか、あるいは肝転移が単発で腫瘍を取りきれると判断されること、などを条件としています。
膵癌・胆道癌
膵癌・胆道癌の肝転移は治療に奏効することがほとんどなく、診断時がついた時点で余命が限られている場合が多いのが現状です。したがって膵癌・胆道癌の転移については外科的切除でなく抗癌剤による治療が中心となります。
その他
卵巣癌や乳癌など比較的に抗癌剤の感受性の高い腫瘍での肝転移例では、原発巣のコントロールがされており、肝臓以外に転移巣がなければ、積極的に外科切除をしています。
2.内科的治療法
種々の理由により外科的治療が適応とならない場合には内科的治療を行います。
内科的治療にはラジオ波凝固壊死療法(RFA)、皮下埋め込み式リザーバー動注化学療法などがあります。
A) ラジオ波凝固壊死療法(RFA)
ラジオ波を利用し腫瘍を焼灼します。焼灼範囲は3cmとマイクロ波に比較すると広範囲を凝固することができます。2004年4月より保険適応となりました。
B) 皮下埋め込み式リザーバー動注化学療法
肝動脈に挿入したカテーテルを皮下に埋め込んだリザーバーというタンクを通して抗癌剤注入を行う方法で、リザーバーの留置には2-3日ほど入院が必要です。動注化学療法は外来での施行が可能ですが、抗癌剤の副作用や安全性の確認などの為、はじめは入院にて行うこともあります。合併症は留置したカテーテルの閉塞、移動による消化管に対する抗癌剤の流入による潰瘍形成や潰瘍出血、使用する抗癌剤による副作用(使用薬剤により異なりますので、個々に説明します)などがあげられます。
胆管がんについて
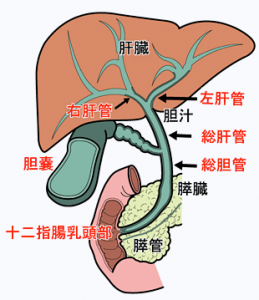
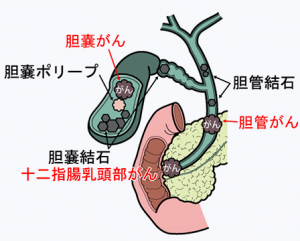
胆管の名称と疾患部位
「胆道」とひとことで言っても、下図のように広い範囲を表します。また、病気の種類やできる場所によって、症状や治療なども大きく変わります。
(図は全て、日本消化器外科学会ホームページ(2024年4月)から引用)
 |
 |
胆管癌について
胆管とは、肝臓で作られた胆汁(消化液の一種)を十二指腸まで流すための管で、その途中に胆嚢があります。これら全体を胆道(たんどう)と呼びます。胆管が肝臓から出たところから始まり、十二指腸にある胆管開口部(十二指腸乳頭といいます)までを指します。したがって、胆道がんには、胆管がん(左右肝管・総肝管・総胆管に発生する悪性腫瘍)、胆嚢がん(胆嚢に発生する悪性腫瘍)、乳頭部がん(胆管の開口部である十二指腸乳頭部に発生するがん)の3種類があります。2022年のがんによる死亡のなかで、肺、大腸、胃、膵、肝についで6位でした。
胆管癌の症状
胆管がんの症状として一番多いものは、黄疸(おうだん:目や体が黄色くなる)で、これはがんのために胆管の通りが悪くなり、胆汁があふれてしまうために起こるもので、閉塞性黄疸と言います。また、これに伴って体のかゆみが出たり、尿の色が紅茶のような濃い色になったり、大便が白っぽくなったりします。患者さん自身が黄疸に気づきにくいことがあり、周囲の人から指摘されて初めてわかることもあります。尿や便の色の異常を感じたときは早めに医師の診察を受けることをおすすめします。
胆管癌の診断
胆管がんの検査は超音波検査、CT、MRI、内視鏡的逆行性胆管造影などを行います。胆管がんはできた場所や広がりによって治療方法(切除術式)が大きく異なりますので、術前の診断は特に重要です。ただし、胆管がんは一見小さな腫瘍に見えても胆管の表面をはっていくような広がり方をしたり、ひきつれが強くてもがんの範囲は少なかったりと様々な形態を示しますので、各種検査を駆使しても正確な診断は困難なことがあります。
胆管癌の治療
胆管がんの治療法としては、現在、手術、化学療法(抗がん剤を使った治療)、放射線治療があります。現在、治癒が望める可能性が一番高いのは手術です。手術の方法は、胆管が肝臓の中から十二指腸にまでおよぶ管という解剖学的な特徴から、がんが発生した部位によってさまざまです。
例えば、肝臓のすぐ近く(肝門部から上部胆管がん)では、肝切除が必要になりますし、中部から下部胆管がんでは、下部胆管が膵臓と接していることから膵臓、十二指腸、場合によっては胃の一部までの切除(膵頭十二指腸切除といいます)が必要になります。いずれにしてもお腹の手術の中では一番侵襲(患者様の身体への負担)の大きい部類にはいる手術が必要な疾患です。当科では、がんの広がりについて詳しい検査をおこない、綿密に評価した上で、安全かつ治癒を目指した積極的な切除をおこなっております。
胆管癌の手術
胆管がんの手術術式は、腫瘍のできた場所や広がりよって異なります。例えば、下の図を参考にしてみてください。
(図は全て、日本消化器外科学会ホームページ(2024年4月)から引用)
| 肝切除+肝外胆管切除について | |
|---|---|
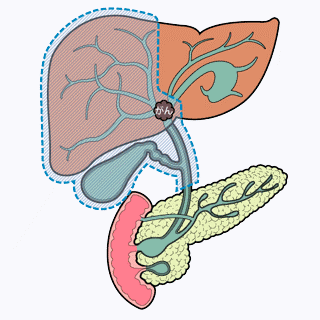 |
肝臓は左と右に大きく分かれていますが、肝門部で肝臓に流入する血管(肝動脈・門脈)も左右に分かれます。肝門部は肝臓の中心であるために、そこにできてしまった腫瘍はなかなか「困った」場所にできてしまった腫瘍と言えます。たいていは肝門部にできたとはいえ、右か左かのどちらかに偏って広がっているので、広がっている方の肝臓を切除します。 このとき中心部にできた腫瘍を取るために、肝臓を部分的に切除することはできませんので、左か右かの肝臓を切除しなければならないのです。さらに肝臓の外の上部〜中部胆管までを切除します。 |
| 膵頭十二指腸切除について | |
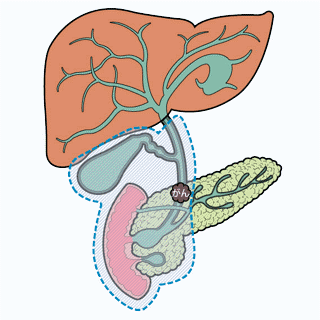 |
胆管の下流は、膵臓を貫いて十二指腸に至ります。こちらの方にがんができてしまった場合は、膵臓への浸潤や、膵臓の周囲へのリンパ節への転移を起こすようになりますので、膵臓の頭部と、そこに付着する十二指腸を一緒に切除しなければなりません。 |
胆管癌の術後経過
肝外胆管を切除した後に、胆管と小腸を吻合(ふんごう:縫い合わせてつなげること)するため、縫合不全(ほうごうふぜん:くっつきが不十分なこと)がなければ、術後2-3日で飲水を開始、数日後に食事を開始します。胆汁漏(縫合または切開した胆管から胆汁が漏れ出ること)、肺炎や創感染(手術した傷が化膿すること)が認められなければ、1-2週間程度で退院になります。
胆管癌手術の合併症とリスク
胆汁漏
胆管を切除した後に、胆管の断端を小腸に吻合して再建するため、吻合部より胆汁が腹腔内に漏れ出ることがあります。ごく少量であれば、自然に軽快することもありますが、通常は漏れ出た胆汁を対外へ排出するためのドレナージチューブの留置が必要となります。
この胆汁漏という合併症には、生命を脅かすほどの危険性はありません。しかし、術後一定の期間、ドレナージ用のチューブの留置が必要となります。全身状態が良好な場合には、退院は十分に可能で、外来通院していただき、外来にてドレナージチューブを抜去することもあります。胆管の吻合部などに狭窄・閉塞(狭くなりつまること)ができて、胆汁の流出が停滞するためおこった胆汁漏に関しては、黄疸(皮膚や眼球結膜が黄染すること)を来すこともあり、胆管の狭窄・閉塞を解除してあげる必要があります。内視鏡を用いて、胆管と小腸の吻合部より逆行性に閉塞・狭窄部をこえてチューブを胆管内に留置して、胆汁をドレナージします。この小腸より留置したチューブは、症状が軽快したら、再び内視鏡を用いて確認しながら抜去します。
胆管炎
こちらも、胆管を切除した後に、胆管の断端を小腸に吻合して再建するため、吻合部を経由して、小腸内の食物残渣や腸液などが、逆行性に胆管へ流入することがあります。このため、胆管内が細菌汚染されることにより誘発されます。
通常、突然の高熱で発症するため、食事をひかえたり中止すること、また抗生剤の治療により症状は軽快します。手術後の炎症などにより、胆管の吻合部などに狭窄・閉塞(狭くなりつまること)ができて、胆汁の流出が停滞するためおこった胆管炎に関しては、胆管の狭窄・閉塞を解除してあげる必要があります。
狭窄・閉塞部位よりも胆管の上流側に、停滞した感染胆汁を排出するために、内視鏡を用いて、胆管と小腸の吻合部より逆行性に閉塞・狭窄部をこえてチューブを胆管内に留置して、胆汁をドレナージします。また、経皮経肝的に肝内胆管にドレナージチューブを留置して胆汁をドレナージすることもあります。ドレナージにより胆管の狭窄・閉塞部の炎症も軽減して、胆管の狭窄・閉塞が解除されて、胆管炎は軽快します。
胆嚢癌について
肝臓で分泌された胆汁を一時貯留しておく胆嚢にできるがんを胆嚢がんといいます。年齢は60-70歳台が最も多く、やや女性に多いがんです。胆嚢がんに胆石の合併する頻度は50-60%です。一方、胆石症に胆嚢がんが合併する頻度は2-3%と低率ですが、高齢者ではもっと頻度が高くなります。膵管胆管合流異常に合併する胆嚢がんが20-30%みられます。 (日本胆道学会ホームページ(2024年4月)から引用)
胆嚢癌の症状
健康診断の腹部超音波検査で、胆嚢に腫瘍様病変が発見される機会が増加しました。胆嚢の腫瘍様病変には胆嚢がん以外にも腺腫や各種ポリープなどの良性病変が数多くみられます。専門医による確実な診断と治療を受けることが大切です。初期は無症状です。進行してはじめて腹痛、発熱、黄疸などが生じます。胆石の合併が多いことから胆石症の症状が前面にでて診断されることもよくあります。がんが進行すると胆汁の通路である胆管を閉塞し黄疸がみられることがあります。
胆嚢癌の診断
診断は超音波検査が第一選択となります。血液生化学検査、腫瘍マーカーを調べます。精査のための画像診断として、内視鏡的逆行性胆道造影、経皮経肝胆道造影、CT、MRI、EUS、IDUSなどを行います。当院では、これらの診断器材、技術のすべてが揃っており早期確定診断をいつでも行えるよう準備しております。
胆嚢癌の治療
治療は、切除可能であれば、外科的手術が最善です。手術法はがんの進展度に従って変わります。がん進展が固有筋層までのものでは、胆嚢摘出術と領域リンパ節郭清でよいとする意見が多いのですが、これ以上の進展度のものでは、胆嚢を中心にしてさらに広い範囲の切除と郭清が必要と考えられております。
抗がん剤による化学療法として当科では、塩酸ゲムシタビン、シスプラチン、デュルバルマブなどを併用して行っております。一般に放射線療法はあまり効果が期待できないといわれていますが、なかには胆管の閉塞が緩和され、閉塞性黄疸が改善する場合があります。
胆嚢癌の手術
手術は胆嚢がんのある場所、浸潤範囲、進行度によって術式が様々です。早期の胆嚢がん(粘膜、固有筋層までの浸潤)であれば胆嚢摘出術のみでよいと言われていますが、漿膜以上の浸潤があった場合は周囲の肝臓、リンパ節、脈管に浸潤することが多いので、胆嚢だけでなく周囲の肝臓やリンパ節を切除する必要があります。その浸潤範囲によって、小範囲の肝切除でよいのか、広範囲の肝切除を行う必要があるのか決定します。進行胆嚢がんの手術は、胆嚢だけでなく周りの肝臓や胆管やリンパ節を切除しなければならないので、おそらく一般の方が想像されるよりも大きな手術になることが多いのです。
胆嚢がんに対する切除範囲は肝胆膵外科の専門家の間でも意見が分かれるところであり、未だ標準的(最適な)な手術術式が定まっていないのが現状です。
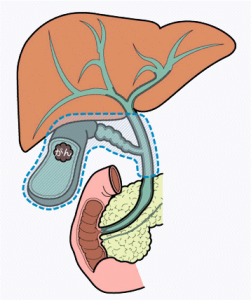
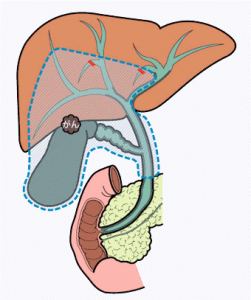
当科の方針としては早期胆嚢がん(粘膜、固有筋層までの浸潤)に対しては腹腔鏡下胆嚢摘出(+肝床切除)、進行胆嚢がんに対しては胆嚢摘出+肝外胆管切除+リンパ節郭清に加えて、肝臓への浸潤範囲によって肝切除(S4a+S5切除)を行い、右肝動脈、門脈に浸潤があるものに対しては拡大右葉切除(肝右葉切除+尾状葉切除)を行っています。
(参考図:日本消化器外科学会ホームページ(2024年4月)より引用)
 |
 |
胆嚢癌の術後経過
術後1-2日目に食事が開始され、創の抜糸後、術後7日目前後に退院されます。進行胆嚢がんでは、肝外胆管を切除した場合には、胆管がんと同様に、胆管と小腸を吻合(縫合してつなげること)するため、縫合不全(縫合が不十分なこと)がなければ、術後2-3日で飲水を開始、数日後に食事を開始します。胆汁漏(縫合または切開した胆管から胆汁が漏れ出ること)、肺炎や創感染(手術した傷が化膿すること)が認められなければ、1-2週間程度で退院になります。
胆嚢癌の術後合併症と手術リスク
胆汁漏
胆管を切除した後に、胆管の断端を小腸に吻合して再建するため、吻合部より胆汁が腹腔内に漏れ出ることがあります。ごく少量であれば、自然に軽快することもありますが、通常は漏れ出た胆汁を対外へ排出するためのドレナージチューブの留置が必要となります。
この胆汁漏という合併症には、生命を脅かすほどの危険性はありません。しかし、術後一定の期間、ドレナージ用のチューブの留置が必要となります。全身状態が良好な場合には、退院は十分に可能で、外来通院していただき、外来にてドレナージチューブを抜去することもあります。胆管の吻合部などに狭窄・閉塞(狭くなりつまること)ができて、胆汁の流出が停滞するためおこった胆汁漏に関しては、黄疸(皮膚や眼球結膜が黄染すること)を来すこともあり、胆管の狭窄・閉塞を解除してあげる必要があります。内視鏡を用いて、胆管と小腸の吻合部より逆行性に閉塞・狭窄部をこえてチューブを胆管内に留置して、胆汁をドレナージします。この小腸より留置したチューブは、症状が軽快したら、再び内視鏡を用いて確認しながら抜去します。
胆管炎
こちらも、胆管を切除した後に、胆管の断端を小腸に吻合して再建するため、吻合部を経由して、小腸内の食物残渣や腸液などが、逆行性に胆管へ流入することがあります。このため、胆管内が細菌汚染されることにより誘発されます。
通常、突然の高熱で発症するため、食事をひかえたり中止すること、また抗生剤の治療により症状は軽快します。手術後の炎症などにより、胆管の吻合部などに狭窄・閉塞(狭くなりつまること)ができて、胆汁の流出が停滞するためおこった胆管炎に関しては、胆管の狭窄・閉塞を解除してあげる必要があります。
狭窄・閉塞部位よりも胆管の上流側に、停滞した感染胆汁を排出するために、内視鏡を用いて、胆管と小腸の吻合部より逆行性に閉塞・狭窄部をこえてチューブを胆管内に留置して、胆汁をドレナージします。また、経皮経肝的に肝内胆管にドレナージチューブを留置して胆汁をドレナージすることもあります。ドレナージにより胆管の狭窄・閉塞部の炎症も軽減して、胆管の狭窄・閉塞が解除されて、胆管炎は軽快します。
膵がんについて
はじめに 通常型膵癌とは、当院の膵切除実施状況
膵腫瘍には、上皮性腫瘍と血管腫リンパ管腫などの非上皮性腫瘍に大きく二分されます。大多数は上皮性腫瘍であり、外分泌腫瘍と内分泌腫瘍に分けられます。外分泌腫瘍には、漿液性嚢胞腫瘍、粘液性嚢胞腫瘍、膵管内乳頭粘液性腫瘍、腺房細胞腫瘍浸潤性膵管癌が有りますが、浸潤性膵管癌が通常型膵癌、いわゆる膵癌です。膵がんとは膵臓から発生した悪性腫瘍のことを指しますが、一般には膵管癌のことを言います。膵管癌は膵管上皮から発生し、膵臓にできる腫瘍性病変の80-90%を占めています。全国統計では肺がん、大腸がん、胃がんについで死因の第4位でした。わが国の膵癌は近年増加傾向にあり、毎年3万人以上の方が膵癌で亡くなっています。膵癌の死亡数はこの30年で8倍以上に増加しました。60歳代の方に多く、やや男性に多く発症します。喫煙、膵癌の家族歴、糖尿病、慢性膵炎などとの関連が指摘されています。2007年の膵癌登録報告によると、全Stage及びStage不明例を含む通常型・組織型不明の浸潤性膵癌全症例の生存率は、1年生存率が1981年-1990年の20.3%から1991年-2000年の25.7%、2001年-2004年の40.2%と飛躍的に改善していますが未だ予後不良の疾患です。
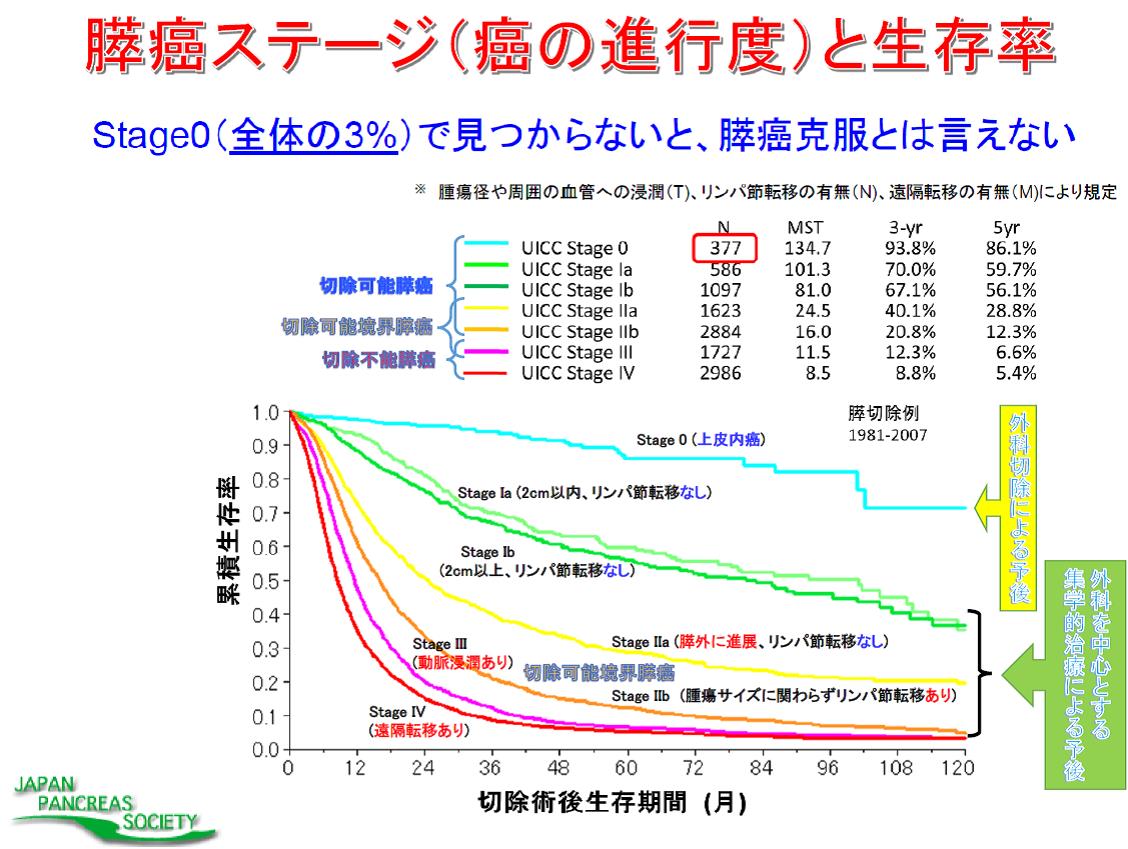
膵癌のスクリーニング法は確立されておらず、早期診断は困難とされています。特定の自覚症状に乏しく、腹痛、背部痛、体重減少、食欲低下、黄疸、特に近年では糖尿病の悪化などを契機に発見されることが多いとされており、膵癌患者数は年々増加傾向であります(下図がん統計参照)。切除可能膵癌として発見される患者は全体の約30~35%にとどまるとの報告があり、膵癌を疑う所見、徴候などございましたらできるだけ早く専門医の在籍する病院の受診を強くお勧めします。
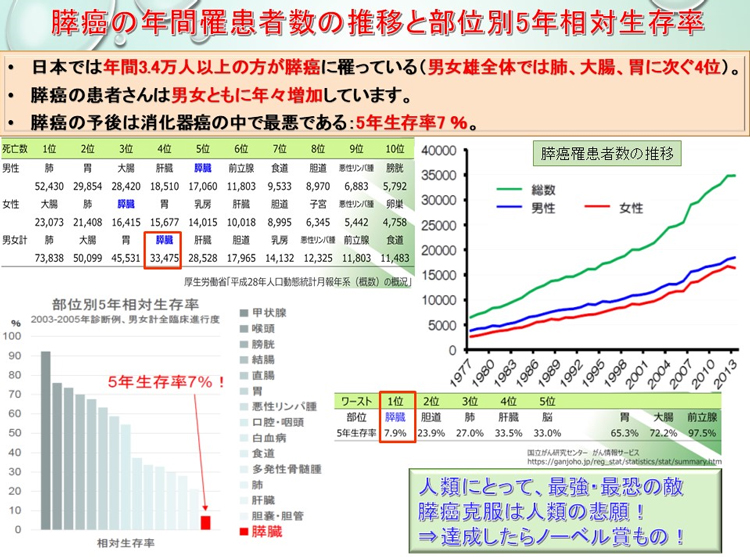
当院 消化器外科には肝胆膵外科高度技能指導医・専門医が在籍し、消化器内科と密接に連携し、根治を目指した膵癌治療にあたっています。黄疸などの症状が発現している患者さんにつきましては、随時、緊急入院していただき必要な減黄処置を実施する体制を整えております。遠慮なくおたずねください。当科では、年間約20例の膵癌症例を手術し膵癌の根治を目指しています。
また、膵癌は外科的切除のみで根治を目指すことは困難とされ、根治を目指した新しい治療法として術前に化学放射線療法または化学療法を行い、再評価の後、膵癌の根治切除を行い、術後補助化学療法を行っており、予後の改善、再発抑制に取り組んでいます(下記に詳細を述べています)。
さらに膵切除術では、腹腔鏡を用いた低侵襲手術にも積極的に取り組んでいます(下記術後写真参照)。手術は、内視鏡外科学会技術認定医の執刀の元、安全に施行しております。
膵癌を含めた膵疾患の外科的治療についてのご相談は、消化器外科 肝胆膵グループにご確認ください。
 |
 |
膵癌の正確な病期診断
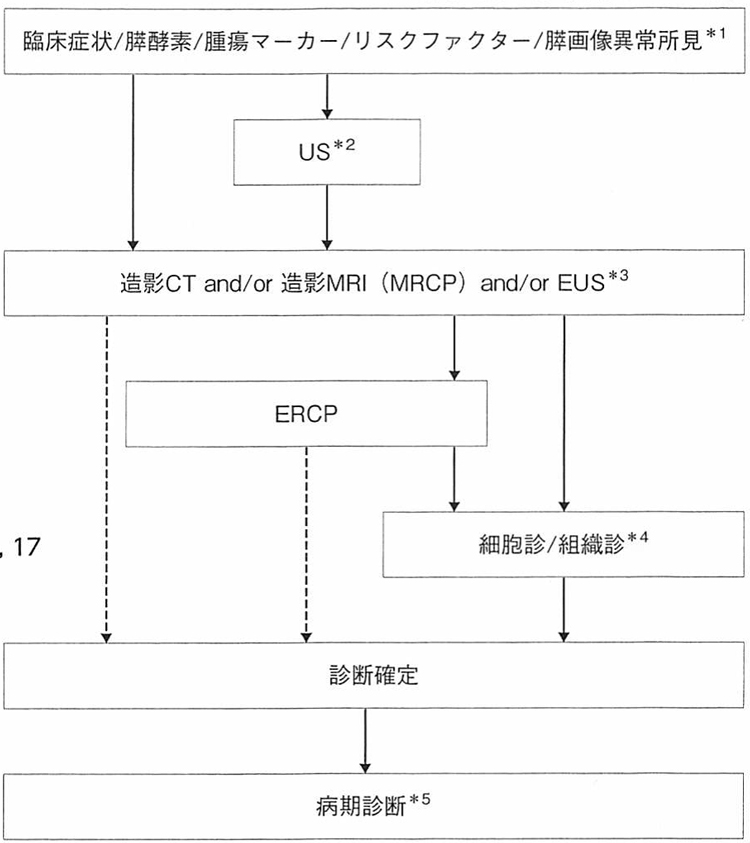
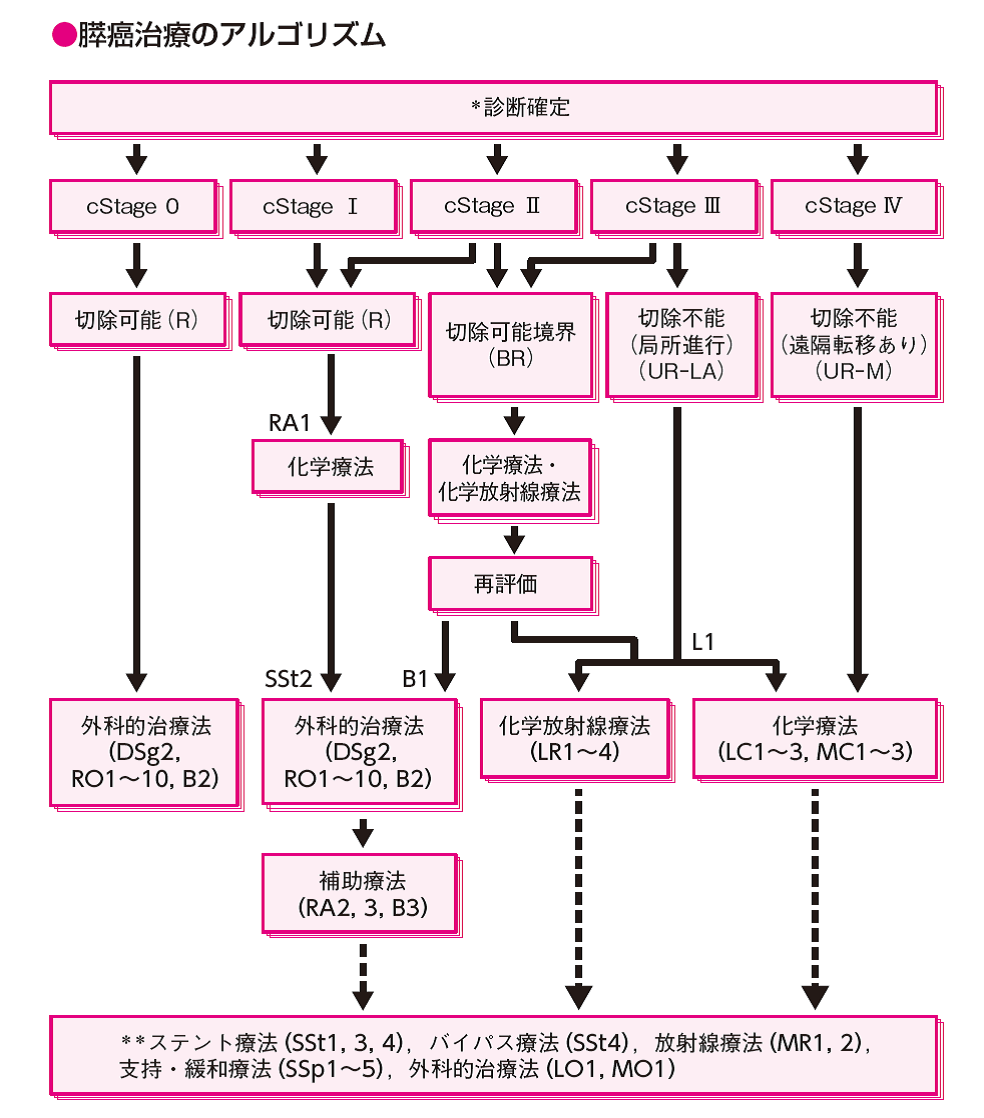
当院、消化器外科・消化器内科では、「科学的根拠に基づく膵癌診療ガイドライン」に基づき診断・治療しています(図1)。治療方針は「原発性膵癌取扱規約」の進行度分類により変わってきます。そのため正確な病期診断が必要になります。まず臨床症状、膵酵素/腫瘍マーカー(CEA, CA19-9, DUPAN-2, Span-1)/危険因子、超音波検査を行い、次に造影CTおよびMRI(MRCP)を施行し、これらの画像診断所見より膵腫瘍の存在診断をしています。さらに、内視鏡的逆行性膵管造影(ERCP)、超音波内視鏡(EUS)、超音波内視鏡下生検(EUS-FNA)を行い膵腫瘍より膵液、腫瘍細胞を採取し膵癌の確定診断を行っていきます。また、遠隔転移、腹膜播種などの全身的診断としてPET-CTが有用とされています。
以上のような検査を総合して膵癌の状態、進行度を把握し、治療法を検討します。
当院では、膵癌診断に必要なすべての検査が実施可能です。
図1 「膵癌診療ガイドライン」による膵腫瘍の診断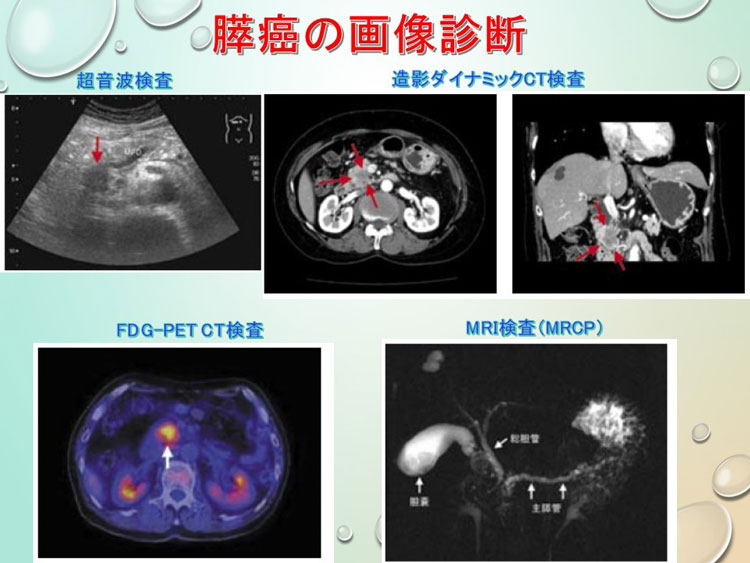
| IA期 | 大きさが2cm以下で膵臓内に限局している。膵外への転移なし。 |
| IB期 | 大きさが2cmを超えているが膵臓内に限局している。膵外への転移なし。 |
| IIA期 | がんは膵臓外に進展しているが腹腔(ふくくう)動脈や上腸間膜動脈に及ばない。膵外への転移なし。 |
| IIB期 | 領域リンパ節への転移あり。しかし、がんは膵内に限局、あるいは膵外に進展しても腹腔(ふくくう)動脈や上腸間膜動脈に及ばない。 |
| III期 | がんは膵臓外に進展し腹腔(ふくくう)動脈や上腸間膜動脈に及ぶ。リンパ節転移は問わない。 |
| IV期 | 離れた臓器への転移がある。 |
膵癌の治療
治療は膵がんの進行度や患者さん自身の体力や健康状態によって異なります。手術は最も効果が期待できる治療法で、「科学的根拠に基づく膵癌診療ガイドライン」の治療選択に基づき、StageI, II, IIIでは外科切除を行います。術式は、膵頭部癌に対しては膵頭十二指腸切除(図2)を、膵体尾部癌に対しては膵体尾部切除を行います。腫瘍切除に加え術後のQOLを損なわない範囲のリンパ節郭清と、腹腔動脈・上腸間膜動脈周囲神経叢の半周郭清を実施しています。しかし、手術で取りきれる範囲を越えて膵がんが進行している場合は、手術よりも化学療法や放射線治療が優先されることもあります。
膵癌に対する根治手術は高難度手術であり、手術関連死は1~3%程度と報告されており、肝胆膵手術の専門医が在籍する施設での治療が勧められています。当院では、肝胆膵高度技能指導医・専門医が在籍しており、安心して治療を受けていただくことが可能です。
図2 膵頭十二指腸切除術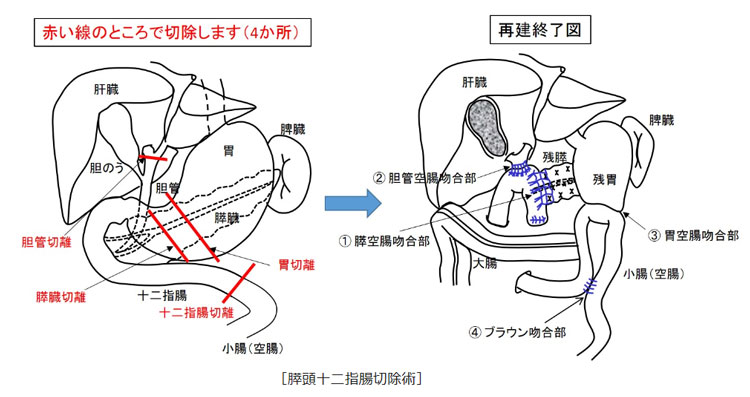
下記に現在の当科の治療方針をお示しします。
| ステージ(取扱い規約8版) | 当科の治療方針 | |
| 切除可能 | IA期, IB期, IIA期, IIB期 | 術前化学療法 → 手術 → 術後化学療法ののち経過観察 |
| 切除可能境界 | III期(切除可能境界) | 化学(放射線)療法 → 手術 → 術後化学療法 |
| 切除不能 (局所進行) |
III期(局所進行切除不能) | 化学(放射線)療法 →(可能な場合は手術Conversion Surgery) |
| 切除不能 (遠隔転移) |
IV期 | 化学療法(下記参照) |
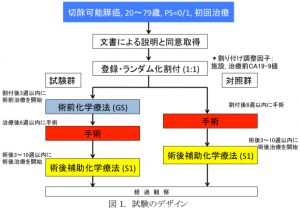
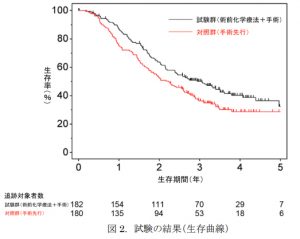
切除可能膵癌に対しては、術前化学療法ののち、外科的切除術を行います。これは、塩酸ゲムシタビンとS-1の変容療法(GS療法)による術化学療法の有用性を評価するためのランダム化比較試験(Prep-02/JSAP05試験)の結果が、2019年1月にサンフランシスコにおいて開催されたASCO-GIにおいて発表されました。そのことから、当院でも術前化学療法を施行後、手術を行っています。
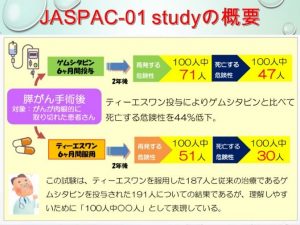
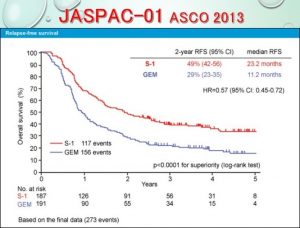
外科的切除がなされた後は、術後補助化学療法を約6か月追加しています。術後補助化学療法は、日本で施行された無作為比較試験(膵がん切除後の補助化学療法における塩酸ゲムシタビン療法とS-1療法の第Ⅲ相比較試験「JASPAC-01試験」Randomized phase III trial adjuvant chemotherapy with gemcitabine vs. S-1 in patients with resected pancreatic cancer)でTS-1による術後補助化学療法群で有意に無再発生存期間を延長したことから、TS-1 80-120mg/日4週投与2週休薬を基本に4コース6ヶ月間施行しています。しかし、下痢などの消化器症状が強く発現する患者さんではゲムシタビンを用いた補助療法に変更することもあります。
 |
 |
| Prep-02/JSAP05試験 | |
 |
 |
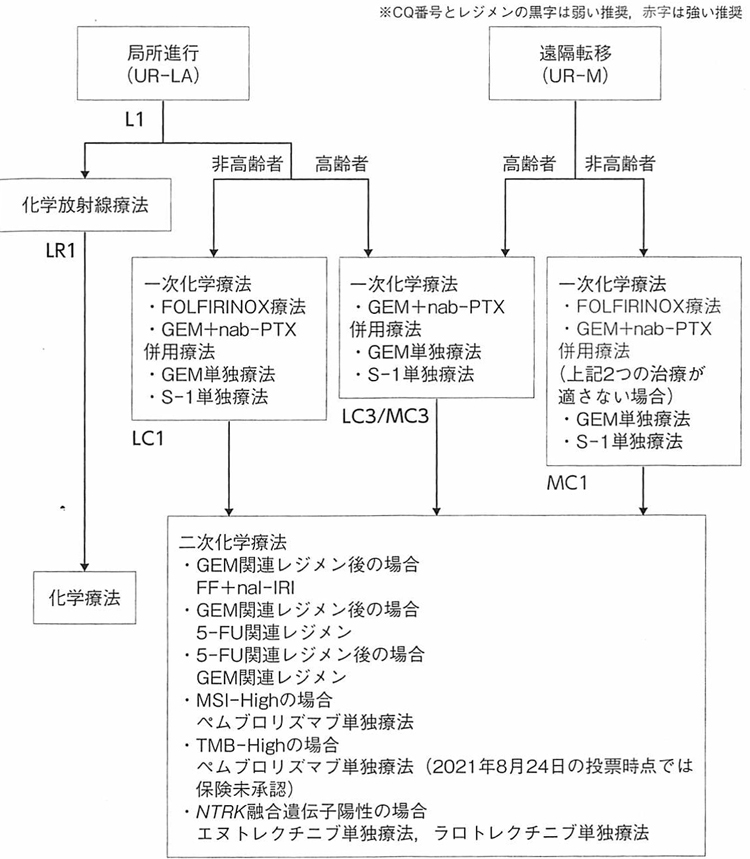
StageIVは、すでに遠隔転移を持つ切除不能膵癌です。全身状態が良好であれば、ゲムシタビン、アルブミン懸濁型パクリタキセル(アブラキサン)やTS-1、さらに強力なFOLFIRINOX療法(オクザリプラチン+イリノテカン+5-FU+レボホリナート)による全身化学療法を施行しています(下図参照)。残念ながら全身状態が不良で治療が困難な場合は、除痛など緩和療法を行うことになります。ゲムシタビンやTS-1と他の化学療法剤を併用する事により生存期間を延長できるかは、臨床試験が多数行われており、いくつかの期待される薬剤が有ります。ゲムシタビンと分子標的治療薬との併用については、上皮成長因子受容体(EGFR)のチロシンキナーゼ阻害剤であるエルロチニブ(Erlotinib)との併用で僅かですが生存期間の延長が証明されています(J Clin Oncol.;25(15):1960-6, 2007)。エルロチニブ(タルセバ)は、使用施設が限定されていますが、当院では使用可能です。
また、京都大学、本庶教授のノーベル賞受賞で注目されて抗腫瘍効果が期待されます免疫チェックポイント阻害剤キイトルーダについても使用適応試験を受けていただき適応と判断されれば使用可能です。
 |
局所進行膵癌とは
がんが膵臓の表面を越えて周囲の大事な血管、および血管周囲へ浸潤しており、かつ遠隔転移を伴わない状態の膵がんのことを局所進行膵がんと呼びます。
このうち周囲の血管への浸潤のため切除を行ったとしても、悪性細胞が遺残すると考えられる場合は局所進行切除不能膵癌と呼びます。
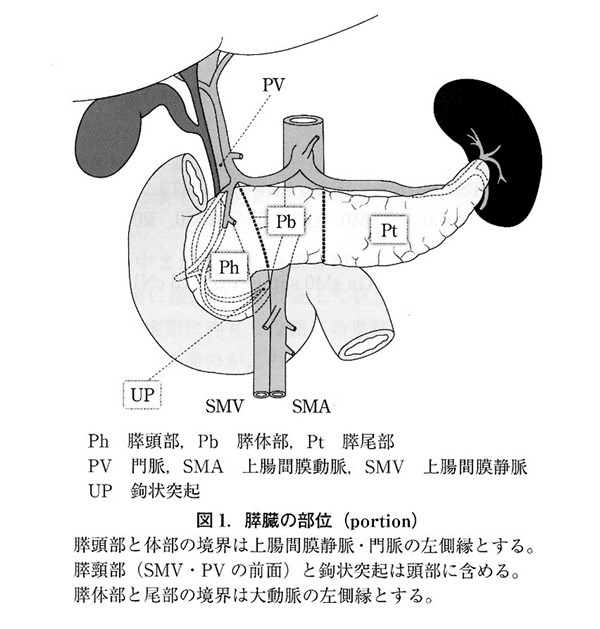
膵癌の診断はしばしば難しい場合があります。これは、他のがんにたとえると、胃がんや大腸がんは胃カメラ・大腸カメラで直接観察して、必要があれば生検鉗子で細胞を採取して顕微鏡で見てがん細胞かどうかを病理診断することができます。しかし、膵臓は腹腔鏡や開腹すれば見えますが、いわゆる胃カメラ、大腸カメラで観察することはできませんので、CTやMRIなどの画像検査によって診断するしかありません。(別の項目で解説してありますが、超音波検査ができる胃カメラから針生検を行って膵癌を診断することはその中で有力な方法です。)治療方針を決めるにあたっては、膵癌がどこまで広がっているかが大切になります。膵臓周囲の血管の近くに腫瘍が浸潤しているかを高精細なCTを用いて診断をします。
局所進行膵癌のうち、重要な動脈に浸潤しているか、もしくは門脈への浸潤程度によって、「切除不能 Unresectable」とよび、切除の可能性が残る「切除不能境界 Borderline resectable」と区別しています。
血管の周りにがんが近接している場合、単に接しているだけなのか浸潤している状態なのかを画像所見で判断しなくてはなりませんがこれはときに困難です。同様に、がんによる浸潤なのか炎症など別の理由で画像の変化が起こっているのかどうかを判別することも困難な場合があります。
手術が可能かどうかを判断するときに2つのことを考える必要があります。まず、技術的に可能かどうかという点、これは安全性と直結します。次に、手術をしたことによって癌治療として効果的かどうかということです。局所進行膵癌はこの観点から「切除可能性」を慎重に検討されています。仮に技術的に切除できたとしても、根治性が低く再発率が高く、生存予後に良い成績をもたらさない場合は切除が有効とは言えません。手術をすることが本当に良いことなのかどうかを膵癌専門医と一緒に慎重に考える必要があります。
最近、膵癌に対して効果のある抗がん剤が増えてきました。そのため、発見当時は切除不能であっても、抗がん剤治療を行って腫瘍を縮小、或いは勢いを抑え込んでから切除を行うConversion surgery(適当な日本語がありません)という概念が提唱されています。また、ある程度進行している膵癌に対しては、仮に「切除可能境界」の段階でも手術を先行するのではなく化学療法を先行した方がよいという意見が大勢を占めるようになってきました(Neoadjuvant化学療法)。(Prep-02/JSAP05試験)
局所進行膵癌に対する新しい治療:IMRTを応用した術前化学放射線療法
―患者様に優しい膵癌根治療法の確立を目指して―
これまで、がんに放射線の量(線量)を集中させる様々な方法が追究されてきました。しかしながら従来の方法では、がんと感受性の高い正常組織(小腸、十二指腸、骨髄など)が複雑に近接する場合、がんだけに十分照射することはできませんでした。特に、膵臓は後腹膜臓器であり、膵周囲には胃、十二指腸、腎臓、大動脈など放射線照射に対する感受性がやや高い重要臓器が膵臓を取り囲んでいます。これを克服するため強度変調放射線治療(Intensity Modulated Radiation Therapy:IMRT)が開発されました。IMRTとは、最新のテクノロジーを用いて照射野内の放射線の強度を変化(変調)させて照射を行なう方法のことを指します(当院で使用している実際の放射線照射装置:図1)。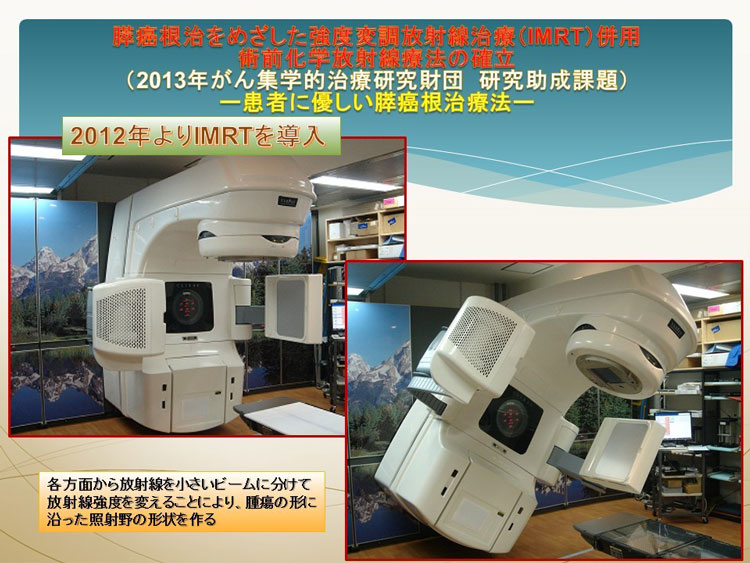
IMRTを使えば、がんの形に凹凸があってもその形に合わせた線量分布が作ることができます(従来の放射線治療とIMRTによる線量分布の比較:図2)。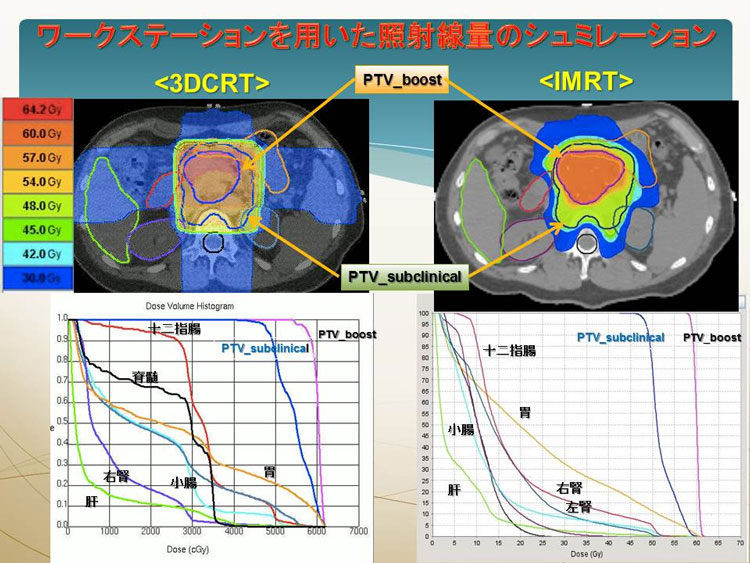
IMRTは、日本でも2000年頃より開始され、2006年には先進医療に認められました。当院では、2010年よりIMRTを導入し、前立腺癌、脳腫瘍から治療を開始し、順次、頭頸部癌、骨盤内臓器での癌に対する放射線治療へと適応を拡大してきました。
2014年から膵癌に対する術前放射線化学療法に応用し、切除率の向上、長期生存率の延長を目指し、癌患者さんに優しい治療を行っています(当院の術前化学療法の治療スケジュール:図3)。本治療の適応、治療効果、治療スケジュールなど詳しい情報は、外科、肝胆膵専門医にお聞きください。
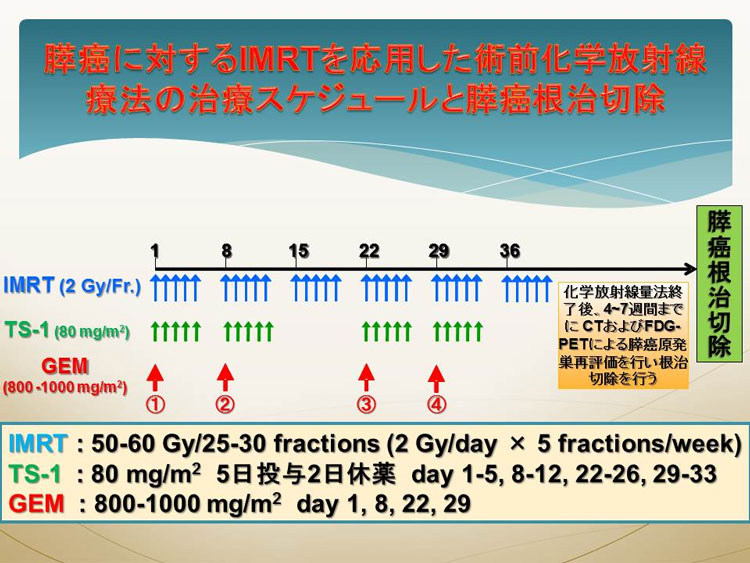
下記に、IMRTを用いて術前放射線化学療法を行い、膵癌根治切除できた症例のCT、PETをお示しします(図4)。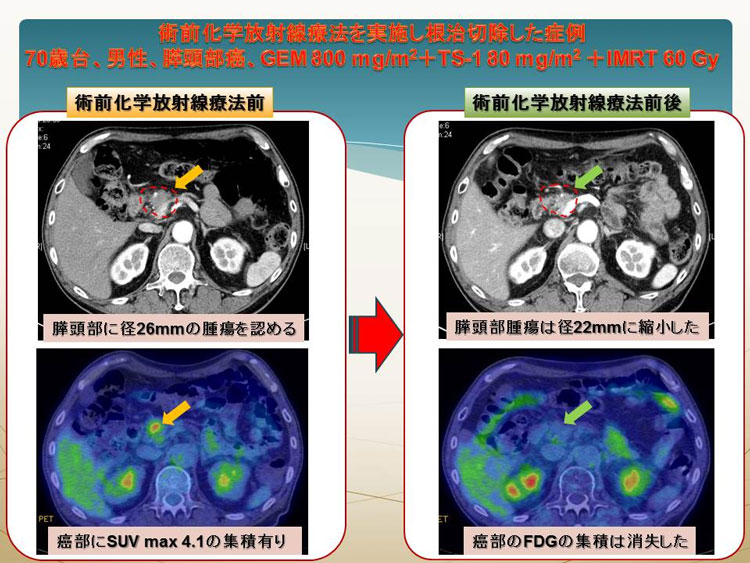

膵管内乳頭粘液性腫瘍(IPMN)について
膵管内乳頭粘液性腫瘍(IPMN)とは
膵嚢胞には炎症性嚢胞と非炎症性嚢胞があり、非炎症性嚢胞の多くは腫瘍性嚢胞です。腫瘍性嚢胞の内、漿液を産生する漿液性嚢胞腫瘍は、ほとんどが良性腫瘍です。一方粘液を産生する嚢胞性膵腫瘍は、膵管内乳頭粘液性腫瘍(IPMN)と粘液性嚢胞腫瘍(MCN)に分類されます。膵管内乳頭粘液性腫瘍(IPMN)は、当初は良性の膵管内乳頭粘液性腺腫ですが、時間経過とともに、膵管内乳頭粘液性癌、膵管内乳頭粘液性腫瘍由来浸潤癌と変化していきます。
膵管内乳頭粘液性腫瘍(intraductal papillary mucinous neoplasm:IPMN)は、上記のように膵囊胞性疾患のひとつであり,その形態から分枝型,主膵管型および混合型に分類されます(図1)。分枝型は「主膵管と交通する5mm以上の分枝の拡張」と定義され、主膵管型は「ほかに原因のない部分的あるいは全体的な5mm以上の主膵管拡張」,混合型は「主膵管型と分枝型の特徴を併せ持つもの」と定義されます。IPMNは組織学的に,良性であるIPMN with low-grade dysplasiaと,悪性であるIPMN with high-grade dysplasia(HGD),IPMN with an associated invasive carcinoma(INV)に分類され,特にINVは通常型膵癌と同様に予後不良とされています。
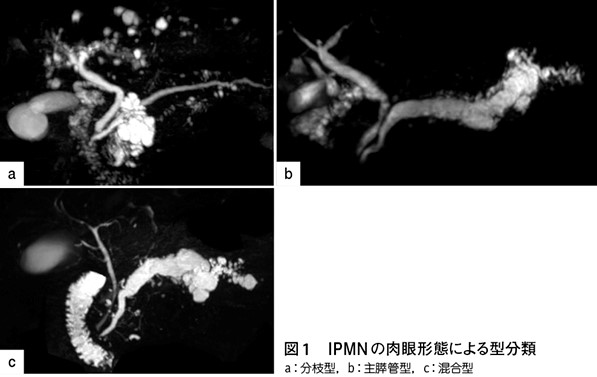
膵管内乳頭粘液性腫瘍の治療
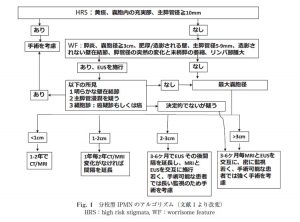
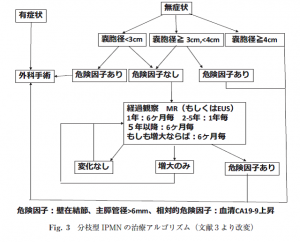
当科では、下記に示すようにIPMN/MCN国際診療ガイドラインに準拠し手術適応を決定し、切除しています。また、無症候性膵腫瘍性のう胞を指摘された患者さんに対しても必要な検査を行いながら当院で経過観察いたします。
 |
 |
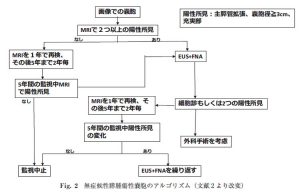 |
外科的切除の方法ですが、膵頭部側(十二指腸側)の腫瘍は膵頭十二指腸切除を施行しています。膵尾側(脾臓側)の腫瘍は、浸潤癌の場合は、通常型膵癌と同じく郭清を伴う膵尾側切除を施行しています。浸潤癌で無い膵体尾部のう胞の場合は、低侵襲で整容性にも優れた腹腔鏡下膵体尾側切除を、内視鏡外科学会技術認定医の執刀の元、安全に施行しております。術式の適応・選択については外科、肝胆膵外科専門医にお聞きください。
腹腔鏡下膵尾側切除の手術創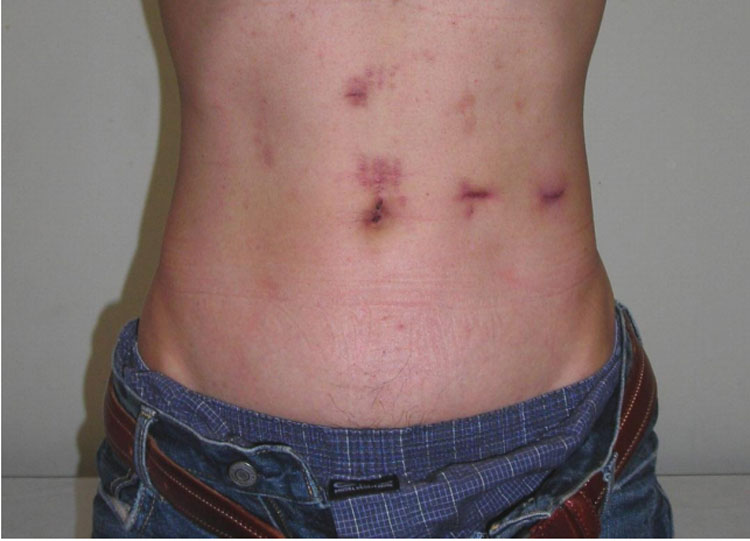
膵神経内分泌腫瘍(P-NET)について
膵神経内分泌腫瘍(P-NET)とは
神経内分泌腫瘍(neuroendocrine tumor; NET)は、消化管や内分泌組織に広く分布する神経内分泌細胞由来の腫瘍です。膵臓では膵ランゲルハンス島と呼ばれる部分があり、様々な膵内分泌ホルモンを産生しています。その様な膵ランゲルハンス島の細胞由来の腫瘍が膵内分泌腫瘍です。インシュリンを産生するインシュリノーマ、ガストリンを産生するガストリノーマ、グルカンゴンを産生するグルカンゴノーマ、ソマトスタチンを産生するソマトスタチノーマなど、ホルモンによる症状を起こす症候性膵島腫瘍と、ホルモンによる症状を起こさない無症候性膵島腫瘍が有ります。無症候性膵島腫瘍には、非機能性膵内分泌腫瘍も含まれます。進行は比較的穏やかですが、急激に進行するものもあり、注意が必要です。最近ではiPhoneで有名な Apple社のCEO スティーブ・ジョブズ氏が罹患した病気です。膵NETの年間初診数は人口10万人あたり2.7人と稀な疾患です。また多発性内分泌腫瘍症(MEN)に合併する場合もあり、全身検索も必要です。
NETと遺伝との関係ですが、遺伝のものと遺伝ではないものがあります。遺伝の場合はMEN-I型、VHL(フォンヒッペルリンドウ病)などがあります。診断と治療は遺伝子の種類によって変わって来 ますのでさらに専門的な判断が必要になります。
膵神経内分泌腫瘍の診断
ホルモンによる症状を有する機能性膵内分泌腫瘍である、ガストリノーマ(Zollinger-Ellison症候群)、インスリノーマ、グルカゴノーマ、ソマトスタチノーマ、VIP腫瘍(Verner-Morrison症候群)、GRF腫瘍(Growth-hormone-releasing factor)、ACTH産生腫瘍など機能性膵内分泌腫瘍の診断は、産生するホルモンの高値により診断します。下記に機能性NETの一覧を掲載いたします。
機能性NETの一覧
|
NETの名称 |
産生される |
症状 |
頻度の高い |
悪性の |
|
インスリノーマ |
インスリン |
動機、冷や汗、意識障害などの低血糖症状 |
膵 |
5~10% |
|
ガストリノーマ |
ガストリン |
繰り返す消化性潰瘍 |
膵、十二指腸、胃 |
90% |
|
VIPオーマ |
VIP |
激しい水様性下痢、電解質の異常(低カリウム血症) |
膵、十二指腸 |
75% |
|
グルカゴノーマ |
グルカゴン |
糖尿病、体重減少、貧血、移動性紅斑 |
膵 |
50% |
|
セロトニン産生腫瘍 |
セロトニン |
皮膚の紅潮、下痢、心臓病、喘息症状 |
全消化管、呼吸器、膵 |
100% |
|
ソマトスタチノーマ |
ソマトスタチン |
糖尿病、脂肪便、胆石 |
膵、十二指腸 |
50% |
2010年のWHO分類により、膵・消化管神経内分泌腫瘍は、Neuroendocrine Neoplasm(NEN)と総称され、核分裂像数(10HPF当たりの核分裂像数)とKi-67指数(細胞増殖関連抗原Ki-67に対するMIB-1抗体標識率)からG1~G3に悪性度分類が提唱され、特にG3は神経内分泌癌(Neuroendocrine carcinoma; NEC)とされています。さらに、この悪性度分類を改良したWHO 2019年分類が出ました。
|
WHO 2019分類 |
||
|
Ki-67 index |
Mitotic index |
|
|
Well differentiated NET G1 |
< 3 % |
< 2 /10 HPF |
|
Well differentiated NET G2 |
3-20 % |
2-20 /10 HPF |
|
Well differentiated NET G3 |
>20 % |
>20 /10HPF |
|
Poorly differentiated NEC G3 |
||
|
Small cell type |
||
|
Large cell type |
||
|
Mixed neuroendocrine non-neuroendocrine neoplasm (MiNEN) |
||
NETの診断は?
症状がある機能性NETの局在診断
機能性NETの場合、異常に産生されるホルモンによる特徴的な症状が、NET診断のきっかけになります。 例えば、頻度が最も高いインスリノーマの場合、血糖が低いことや、空腹時の血液中のインスリン濃度が高いことなどが診断となります。
機能性NETの診断の特徴的な検査法として、血管造影を利用した選択的動脈内カルシウム注入法(Selective arterial calcium injection test,SACI試験)という負荷試験があります。画像診断で腫瘍の場所がはっきりとわからない場合や多発している場合があり、手術をするためには、NETの部位を正確に診断すること(局在診断)が重要です。SACIテストでは、カルシウムの刺激でホルモンが上がる場所を正確に診断することが可能です。
非機能性NETの局在診断
非機能性NETは、健康診断などで偶然指摘されることが診断のきっかけになります。CT検査やMRI検査で、血流が豊富な腫瘍として発見されます。非機能性のためホルモン活性は持ちません。
膵神経内分泌腫瘍の外科治療
治療には、手術による切除術、薬物療法、局所療法などがあります。手術は、NETに対して最も有効な治療法で、現時点では唯一根治を望むことができる治療です。一方で、他の臓器に転移した場合(特に肝転移)でも、減量手術による機能性症状の緩和や予後の延長が期待できる場合があります。
機能性NETの治療
機能性のNETの場合、基本的に悪性化する可能性があるため手術をおこないます。当院では、通常のがんに準じたリンパ節郭清を含めた膵切除を行っています。
非機能性NETの治療
非機能性NETは、機能性NETと比較すると悪性度が低いことが多く、特に、大きさが2cm未満のNETについては、リンパ節転移がないという報告もあります。そのため、腹腔鏡手術や膵縮小手術(リンパ節郭清を行わない膵部分切除)が行われます。しかし、2cm以下の非機能性NETでも、悪性例の報告もあり、慎重に術式の選択は行う必要があります。
膵神経内分泌腫瘍の薬物治療
肝臓や肺などへの遠隔臓器への転移を認めた場合や、一度の手術できれいに腫瘍がとり切れない大きな腫瘍の場合は、薬物療法が治療の中心となります。NETは、腫瘍の増殖する能力の強さから、NET G1、NET G2、NECに分類され、NETは、低~中悪性度の高分化型の腫瘍である一方、NECは悪性度の高い低分化型の腫瘍です。薬物療法は、NET G1/G2と悪性度の高いNECに分けて、治療方針が異なります。
1.NET G1とNET G2に対する治療
近年、分子標的薬など、膵・消化管原発の神経内分泌腫瘍を中心に新たな薬物療法が開発され、日本でも使える薬が増えてきました。
<分子標的薬 エベロリムス スニチニブ>
分子標的薬は、がん細胞に認める細胞の分裂や増殖に関連したスイッチを治療する薬です。現在は,膵臓のNETに対する分子標的薬として,エベロリムス(アフィニトール)というmTOR阻害剤やスニチニブ(スーテント)といわれる血管新生増殖因子受容体を特異的に阻害するキナーゼ阻害剤などが使用されています。正常な細胞にはあまり影響を与えませんが、抗がん剤にはあまり見られない特徴的に副作用があります。
<ソマトスタチンアナログ>
機能性NETに対する症状を和らげる治療として使用されます。過剰に分泌されているホルモンの分泌を抑えます。また、消化管NETに対して、腫瘍が大きくなるのを抑える効果が示されています。 オクトレオチド(サンドスタチン)は、未治療の局所切除不能または転移性の高分化型NETに対する抗腫瘍効果が示されています(PROMID試験)。海外のデータでは、ランレオチド(商品名 ソマトチュリン)持続性ソマトスタチンアナログ徐放性製剤の有効性も示されており、日本でも適応申請されています。
<ストレプトゾシン>
ストレプトゾシン(ザノサー)は、細胞障害性のニトロウレア系抗悪性腫瘍薬で、DNA合成を阻害することで腫瘍の増殖を抑える作用があります。海外では、エベロリムスやスニチニブなどの分子標的薬が登場する前から使用され有効性が示されています。日本では2015年に製造販売が開始されました。
2.NECに対する治療
NETの中でも、NECは悪性度・増殖の能力が高いため「通常の膵がん」として扱われ、NET G1やG2とまったく異なった疾患として治療が選択されます。NETの中でもNECの患者さんは少なく、極めてまれな病気で有効性が科学的に示された治療法がないのが現状です。そのため、よく似た病気である小細胞肺がんと同じ治療方法が推奨されています。NECの治療は、抗がん剤による化学療法が第一選択で、シスプラチンとエトポシドの併用療法、あるいはシスプラチンとイリノテカンの併用療法などが行われています。
2.NETに対する最新治療
外科的切除ができない神経内分泌腫瘍に対しては、分子標的薬や抗がん剤治療が従来行われてきましたが、2021年、あらたな治療法としてペプチド受容体放射性核種療法(商品名:ルタテラ)が保険承認されました。神経内分泌腫瘍症例の一部に、細胞表面にホルモンの一種であるソマトスタチン受容体が高頻度に発言している場合があります。ペプチド受容体放射性核種療法では、ソマトスタチン受容体陽性の神経内分泌腫瘍に対して、ソマトスタチン類似物質に放射性同位元素であるルテチウム-177を標識した放射性医薬品を投与し、細胞内に取り込まれたルテチウム-177から放出されるベータ線によって治療を行います。治療は点滴注射で行われますが、治療後しばらく体外にガンマ線が放出されるため、原則として専門施設で治療後翌日まで入院が必要です。
その他の膵腫瘍
そのほかにも膵腫瘍にはいろいろな種類がありますが、ここでは主に充実性偽乳頭状腫瘍(SPN)と転移性膵腫瘍について簡単に述べます。
充実性偽乳頭状腫瘍(SPN)の概要
大部分が若年女性に発生する稀な腫瘍で、ほとんどは良性の経過を示しますが、2010年のWHO分類では低悪性度の腫瘍と定義されました。5㎝以上のSPNは悪性とされています。顕微鏡でβカテニンとCD10が陽性、クロモグラニンAが陰性(NETでは陽性)であり、トリプシン、BCL10が陰性(腺房細胞腫瘍で陽性)の所見を認めることが確定診断となります。2013年に出た大規模な研究では、これまでSPNと診断された2744人の90%が最近10年のデータであると発表されました。約9割が女性で平均年齢が約30歳でした。完全切除ができれば再発率が下がるとの報告があります。
転移性膵腫瘍の概要
膵悪性腫瘍の2~5%と言われていますが、実際はもっと多いことが予想されています。ただし、膵切除が予後改善につながるか否かはまだ未解決とされています。最近の18研究399例を見直した研究では、腎細胞がんの転移が6割と最多で、5年生存率は50%(腎細胞がんの場合は70%)、膵外にある場合は予後不良と報告されました。
良性疾患について(胆石、胆のうポリープなど)
胆石症、胆嚢炎、胆嚢ポリープについて
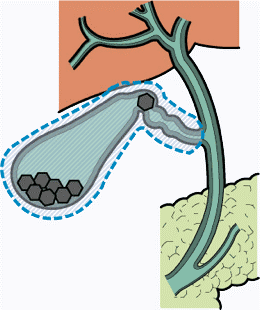
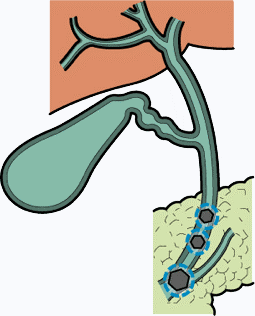
胆石症とは胆石(胆嚢や胆管にできる結石)によって引き起こされる病気の総称です。肝臓で作られた胆汁は一度胆嚢に蓄えられた後、胆管を通って十二指腸に流れます。その胆汁中の成分が析出することにより石となります。多くは胆嚢で石となるためそれを胆石(胆嚢内結石)と呼びます。まれに胆管(肝内胆管、総胆管)に石ができることもあり、それらは肝内胆管結石、総胆管結石と呼ばれます。
 |
 |
胆石を持っている人すべてに症状が出るわけではありません。半分以上の人は胆石を持ちながらも無症状で生活しています。一部の人が胆石による症状、すなわち食後のみぞおち〜右上腹部の痛みを訴えることがあるわけです。それは食事の刺激により石が胆嚢の中で動いたり、場合によっては細菌感染を起こして胆嚢炎を起こすことで症状が出ます。胆嚢炎では右上腹部痛に加え発熱も出現し、全身状態が悪化していきます。ここまでくると入院治療が必要となります。胆嚢炎とまでいかなくとも、症状が出現した人は原則として治療の適応になります。
また、胆管内に石ができた人は症状がない人でも今後症状が出現する可能性が高いため、治療の適応になります。
胆嚢ポリープとは胆嚢内にできたポリープを指します。その多くはコレステロールポリープといって、コレステロールが析出して盛り上がっていく良性のポリープです。それ自体が大きくなっても悪性化することはありません。
ただ、ポリープの中にもごく一部に悪性のものがあり、いわゆる胆嚢癌と言われます。良性のポリープと悪性のポリープの鑑別は、腹部エコー検査やCT,MRI検査でわかることが多いのですが、一部には鑑別が難しいものもあります。特に、ポリープが大きくなってきている場合や、採血検査で腫瘍マーカーが上昇している場合は胆嚢癌を疑って手術で胆嚢を摘出することがあります。また、癌の進行具合によっては追加の手術が必要になることもあります。
胆石症、胆嚢炎、胆嚢ポリープに対する手術
胆石の治療としては手術で胆嚢ごと摘出する方法が第一選択となります。薬で胆石を溶かす方法や衝撃波で石を砕く方法もありますが、成功率、再発率の問題から一般的ではありません。
手術は当院では腹腔鏡による手術を行っています。腹腔鏡手術の利点は体に4か所の小さな傷(5~12mm)をあけて、その傷から細いカメラや鉗子などを挿入して胆嚢を摘出する方法です。利点は傷が小さいため術後の痛みが少ないこと、食事も早期から開始となり体への負担が小さいことなどがあげられます。また、体にあけた小さな傷は縫合して閉じますが、その際には当院では体に吸収される糸を使用しているため抜糸の必要がありません。そのため、手術後2~4日での退院が可能となります。
しかし、腹腔鏡にも弱点があります。カメラ画面を通しての手術となるため、どうしても手術操作に制限がかかってしまうのです。そのため、以前に上腹部の手術をしたことのある方(胃や十二指腸の手術)、ひどい胆嚢炎を起こしている方などは腹腔鏡では手術困難なことが予想され、従来の開腹手術を選択することもあります。
胆石症、胆嚢炎、胆嚢ポリープの術後経過
開腹手術か腹腔鏡下手術かで術後経過は多少異なります。翌日から食事を開始し、病棟歩行も開始します。通常の経過では入れませんが、あればドレーンも翌日に抜去します。腹腔鏡下胆嚢摘出術の場合は術後2〜4日目に退院となることが多く、開腹手術の場合は術後4〜7日で退院となることが多いです。しかし、術後経過は患者さん一人ひとりでかなり幅があります。とくに、胆嚢炎など炎症が強い場合や緊急手術となったような場合は、炎症が治まるのを待ってから退院となりますので、数週間の入院を要することもあります。
胆嚢摘出手術はほぼ安全な手術ですがまれに合併症を起こすことがあります。例えば手術後に出血を起こすこと(後出血)、胆汁が漏れ出すこと(胆汁漏)などです。これらが起こった場合、多くは点滴治療で改善しますが、程度がひどい時には追加処置を行うこともあります。 その他、創感染(傷が膿んでしまう)、肺炎、胆管損傷(胆汁の流れ道を傷つける)、腸管損傷(小腸や大腸を傷つける)などもありますが、どれもまれな合併症です。
また、手術中に高度な炎症性癒着や出血などにより腹腔鏡での手術が困難と判断した場合は、そのまま速やかに開腹手術へ移行することもあります。開腹移行の判断は、執刀しております消化器外科専門医の判断にお任せください。胆管損傷などの修復には高度な手術技術が必要となります。当院では肝胆膵高度技能指導医・専門医が在籍しており的確なバックアップができる体制を整えております。


- 診療科・部門
- 総合内科・感染症内科
- 糖尿病・内分泌代謝内科
- 腎臓内科
- 血液内科
- 肺腫瘍内科
- 脳神経内科
- 循環器内科
- 呼吸器内科
- 消化器内科
- 乳腺内分泌外科
- 消化器外科
- 脳神経外科
- 心臓血管外科
- 整形外科
- 形成外科
- 呼吸器外科
- 小児科
- 産婦人科
- 泌尿器科
- 眼科
- 耳鼻咽喉科・頭頸部外科
- 口腔外科
- 放射線科
- 麻酔科
- リハビリテーション科
- 救急科
- 救命診療科
- 国際センター
- 健康管理センター(人間ドック・健康診断)
- 診療支援局について
- 薬剤部門
- 検査・栄養部門
- 検査部門
- 臨床検査
- 病理検査
- 放射線部門
- 臨床工学・技術部門
- 臨床工学
- 臨床技術
- 感染症センター
- 手術センター
- 心臓・血管センター
- 泉州広域母子医療センター
- 後期研修内容の詳細
- 急性期外科センター
- 高度脳損傷・脳卒中センター
- リハビリテーションセンター
- がん治療センター
- 甲状腺センター
- 糖尿病センター
- 血液浄化センター
- 放射線治療センター
- 聴覚・言語支援センター
- 栄養管理センター
- 機能外傷センター
- ドクターサポートセンター
- 人工関節センター
- 先進医療開発センター(臨床研究・治験・RICWA)
- 臨床研究
- 治験事務局(治験審査委員会)
- 患者サポートセンター
- RICWA(りんくうウェルネスケア研究センター)
- 臨床研修センター
- りんくう総合医療センター看護局
- がん相談支援センター
- 医療相談窓口